Les virus, ces agents infectieux, identifiés aujourd’hui comme « ennemi public n° 1 », semblent aussi pouvoir devenir des alliés contre des pathologies cancéreuses. C’est ce que démontre un groupe de scientifiques américains qui font le point sur les voies de recherche actuelles combinant les thérapies classiques et l’ingénierie génétique.
au sommaire
Les virus oncolytiques, littéralement « virus tueur de cellules cancéreuses », sont connus depuis plus d'un siècle grâce à un premier cas, décrit en 1904, d'une patiente atteinte de leucémie myéloïdemyéloïde en rémission après avoir vraisemblablement contracté une grippe. Qu'ils soient mutés ou sauvages, ils ont l'avantage de se répliquer préférentiellement dans les cellules tumorales et de conduire à leur régression par lyse cellulaire et stimulation de la réponse immunitaireréponse immunitaire tumorale.
Les atouts des virus oncolytiques
Les cellules cancéreuses ont des particularités très spécifiques. Elles produisent beaucoup de nucléotides (pour se reproduire rapidement), elles développent un réseau de vaisseaux sanguins (oxygénation) et ont la capacité de détourner la réponse immunitaire en ne répondant pas à certaines cytokines (interféroninterféron de type 1). De plus, elles brouillent les pistes en produisant à leur surface des protéines capables de provoquer l'inhibitioninhibition des cellules cytotoxiquescytotoxiques (point de contrôle immunitaire). Ce dernier point est d'ailleurs, la clé de voûte des recherches en immunothérapie utilisée dans le traitement de certains cancerscancers.
Ce sont ces différentes particularités qui vont être exploitées dans l'utilisation des virus oncolytiques. Pour être un bon candidat, le virus utilisé doit être peu ou pas toxique pour les tissus normaux, immunogène et cibler préférentiellement les cellules tumorales.
Grâce à l'ingénierie génétiquegénétique, il est possible aujourd'hui de retirer des gènesgènes viraux (knock-out) ou de rajouter des transgènes (knock-in). Ces techniques permettent ainsi de développer des virus transgéniquestransgéniques qui se répliqueront de façon préférentielle dans les cellules malignes. La suppression du gène de la thyminethymine kinasekinase qui oblige le virus à infecter des cellules fortement productrices de nucléotides, l'addition d'un gène codant pour des cytokines stimulant l'activité immunitaire antitumorale n'en sont que quelques exemples.
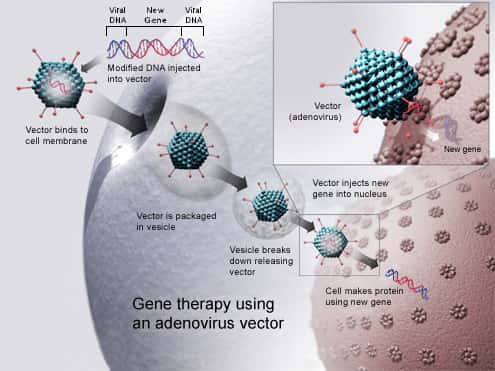
Combinaison de thérapies et de génie génétique
Ces stratégies, à l'étude depuis plusieurs années, rencontrent encore de nombreuses difficultés. Les voies antivirales des cellules tumorales sont encore méconnues et il existe des barrières physiquesphysiques diminuant la pénétration du virus dans les cellules tumorales. De plus, il peut être détruit par les anticorps circulants de l'organisme. Néanmoins, une analyse récente effectuée par des chercheurs américains montre qu'ils peuvent être des alliés précieux, s'ils sont combinés avec d'autres thérapiesthérapies classiques (radiothérapieradiothérapie, chimiothérapie)) ou plus innovante comme l'immunothérapieimmunothérapie par inhibition des points de contrôle (stratégie très prometteuse mais qui ne fonctionne que dans 10 à 20 % des cas). Le génie génétiqueLe génie génétique applicable aux virus oncolytiques en fait des vecteurs d'armement supplémentaires par leur capacité à générer la lyse cellulaire et la stimulation immunitaire.
Aujourd'hui quatre virus oncolytiques sont autorisés dans le monde. Aux États-Unis et en Europe, un virus Herpes simplexsimplex (HSV-1) modifié a été approuvé pour le traitement du mélanome métastasique non opérable. Le virus myxome (provoquant la myxomatosemyxomatose chez le lapin), parce qu'il possède un long génomegénome pouvant intégrer des modifications stables et parce qu'il est inoffensif pour l'Homme, est en cours d'essai préclinique.